

《醫療器械注冊管理辦法》(國家食品藥品監督管理總局令第4號)第四十九條“已注冊的第二類、第三類醫療器械,醫療器械注冊證及其附件載明的內容發生變化,注冊人應當向原注冊部門申請注冊變更,并按照相關要求提交申報資料”;
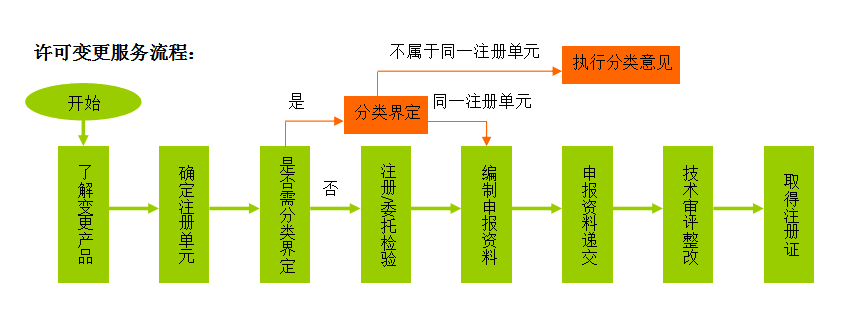
服務項目:
1)確定變更的類型(登記變更、許可變更);
2)(許可變更適用)確定變更產品是否與原獲準產品屬于同一注冊單元;
3)適用時,確定檢驗典型性型號、協助企業快速取得注冊檢驗報告或符合注冊要求的委托檢驗報告;
4)適用時,注冊質量管理體系核查;
5)適用時,臨床評價;
6)主導編制變更注冊所需的申報資料;
7)整理、審核申報資料,并指導企業遞交;
8)技術審評整改(許可變更適用);
9)跟蹤、修訂(必要時)。
注意事項:
1、登記變更:公司名稱、住所、生產地址發生變更;
2、許可變更:產品名稱、產品技術要求(如型號增加或減少、性能指標、檢驗方法等發生實質性變更)
3、注冊變更原則上不進行質量管理體系核查;
4、確定注冊單元、分類界定適用于產品新增結構組成、新增型號等情形;
5、注冊周期視產品種類、檢驗周期(若需要)、是否具備臨床豁免條件以及注冊核查(必要時)是否順利通過等條件限制,根據經驗,周期4~12個月不等(不含臨床試驗,部分產品甚至更長);
Copyright ? 2019 杭州醫咨佳科技有限公司. All rights reserved